有这么一种基因突变
因为缺少针对性的药物
被称为“不可成药”的靶点
然而随着精准医学的高速发展
研究者们终于发现了可以攻克它的药物
为肺癌患者带来治疗的新希望
本期良医汇患者指南邀请到浙江大学医学院附属邵逸夫医院肿瘤内科生金教授撰文为大家科普,KRAS突变晚期肺癌的新希望――靶向治疗。
什么是KRAS突变
肺癌对人类健康构成了巨大威胁,其中最常见的类型是非小细胞肺癌(NSCLC)。KRAS基因是癌症研究中常见的致癌基因之一。正常情况下,KRAS基因编码生成KRAS蛋白,在细胞内扮演着重要角色,参与调节细胞增长、分化等重要生理过程。简单来说,KRAS蛋白就像是细胞内的一个开关,它通过接收外界信号来决定细胞的命运。遗憾的是,当KRAS基因发生突变时,这个开关可能会出现故障,导致它持续处于开启状态。就像是踩下油门的脚无法松开一样,持续激活MAP/ERK信号通路,导致癌症细胞不受控制地增长和转移。
在NSCLC患者当中,约有10%-25%的病例携带KRAS基因突变,主要集中在KRAS第12、13或61号氨基酸位点上,最常见的类型是在第12位点的单点突变。例如KRASG12C突变,即KRAS基因的第12号密码子甘氨酸(G)被半胱氨酸(C)取代形成的突变类型。
携带KRAS突变对患者的预后造成不利影响,生存期较KRAS野生型的患者缩短。同时,由于驱动基因之间的互斥性,KRAS突变的患者很少同时携带EGFR、ALK、ROS-1等靶点,失去了其它已成药靶点精准治疗的机会。更遗憾的是,KRAS突变对传统的治疗方案,例如化疗的敏感性欠佳,很难获得有效且长久的疾病控制。
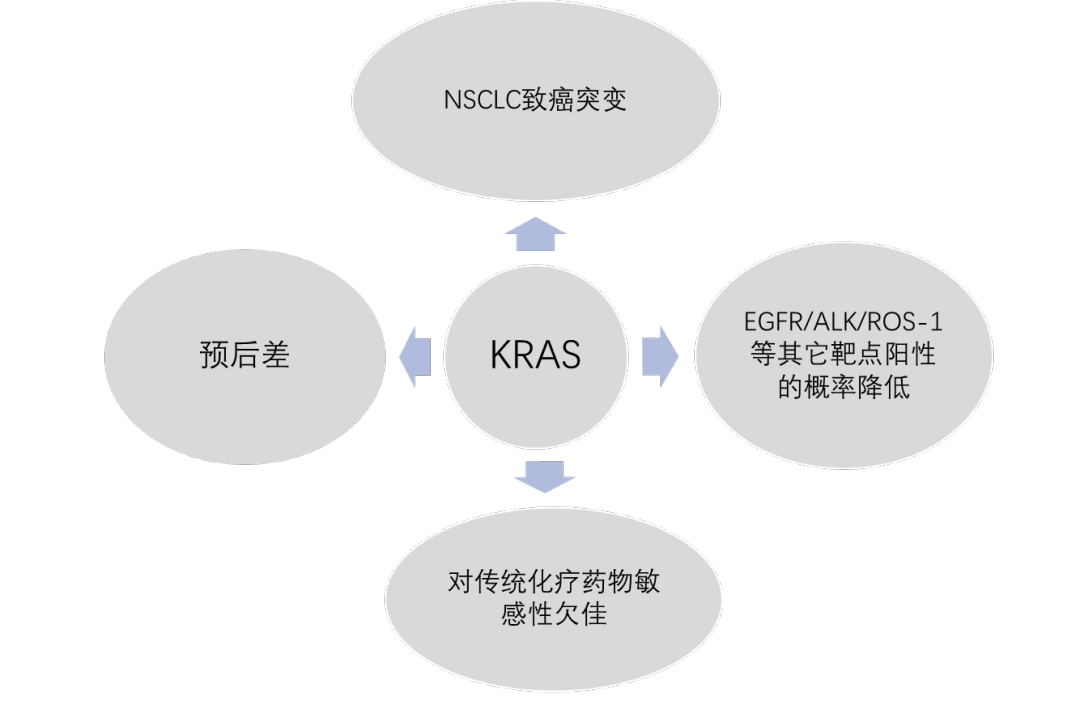
长期以来,由于KRAS蛋白的生物学特性,如其平滑的表面和高亲和性的GTP结合活性,小分子药物很难结合和竞争性抑制,导致KRAS一度被认为是"不可成药"的靶点。然而,近年来,通过尖端的药物设计和筛选技术,研究者终于发现了能够针对KRASG12C突变的小分子抑制剂。这是一个历史性的突破,因为它为治疗携带KRASG12C突变的癌症患者开辟了精准治疗的方向。在临床转化研究和新药开发的过程中,一系列的KRASG12C抑制剂已进入临床研究阶段,帮助数百例肺癌患者改善病情。这些进展为肺癌的个体化及靶向治疗提供了强有力的支持,继续推动着肺癌精准治疗的发展。
当下有哪些KRAS G12C的靶向药物?
索托拉西布(Sotorasib)
索托拉西布是一种口服RAS GTPase家族抑制剂,半衰期为5小时。CodeBreaK 200作为关键的III期研究,纳入了345例含铂化疗、PD-1或PD-L1检查点抑制剂免疫治疗进展的晚期NSCLC患者,试验组为索托拉西布 (960mg 每日一次口服),对照组为多西他赛。该研究达到了主要终点,即索托拉西布中位无进展生存期(PFS)在统计学上显著优于多西他赛(5.6个月对比4.5个月,HR=0.66,p= 0・0017),但两组之间的中位总生存期(OS)未达到统计学意义(10.6个月对比11.3个月,HR=1.01,p=0.53)。索托拉西布相对于多西他赛,显著提高肿瘤的客观缓解率(ORR,28.1% vs 13.2%)和中位持续时间(DOR,8.6 个月vs6.8个月)。索托拉西布最常见的与治疗相关的3级或更严重的不良反应(AE)为腹泻(12%)、丙氨酸氨基转移酶升高(8%)和天冬氨酸氨基转移酶升高(5%)。
阿达拉西布(Adagrasib)
阿达拉西布也是一种口服 RAS GTPase家族抑制剂,半衰期为 23 小时。KRYSTAL-1研究评估了阿达拉西布作为后续疗法对116例KRAS G12C突变阳性晚期NSCLC患者的疗效,这些患者之前接受过含铂化疗±免疫疗法疾病进展。大多数(89%)患者为转移性 NSCLC, 腺癌是最常见的组织学类型(97%)。阿达拉西布单药治疗的中位OS为12.6个月(95% CI,9.2-19.2个月), ORR为42.9%(95% CI:33.5%-52.6%)。颅内反应率为33.3%(95% CI:18.0%-51.8%)。44.8%的患者发生了3级或以上AE,包括贫血、肺炎、呼吸困难、急性肾损伤、低钠血症、疲劳、恶心以及谷丙转氨酶和谷草转氨酶升高。
下表整理了截止2023年12月31日,两种药物已披露的相关信息。
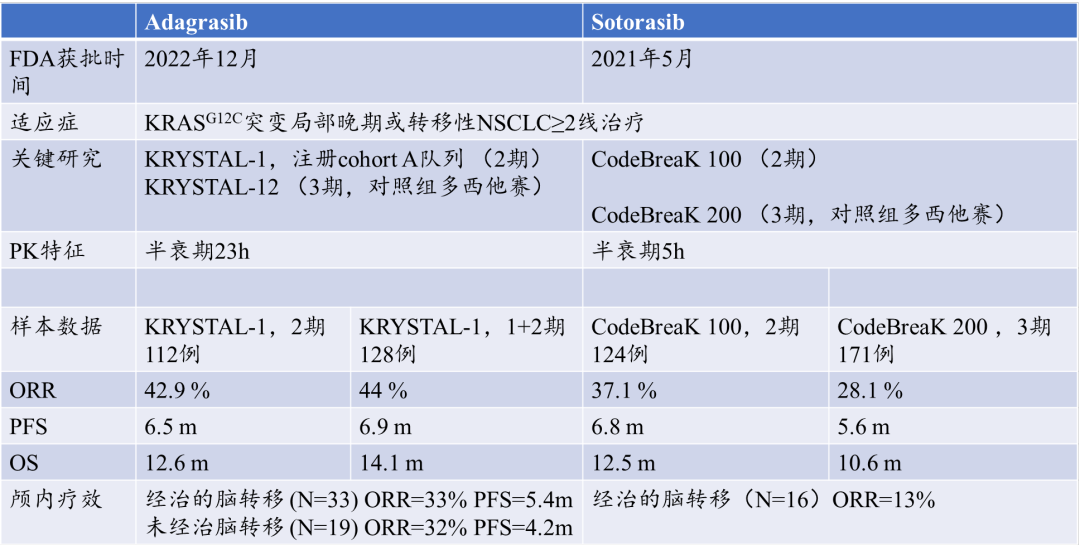
尽管上述两种药物尚未在国内获批上市,但国内靶向KRAS G12C的药物研发正蓬勃开展。例如信达生物的IBI 351,益方生物的D-1553,以及加科思的JAB-21622等,部分已经完成II期临床研究。D-1553获得国家药监局药品评审中心突破性治疗药物的认定,IBI351单药治疗肺癌的上市申请已被受理并获优先审评。在2023年欧洲肿瘤内科学会亚洲年会(ESMO Asia)上公布了IBI351单药治疗肺癌临床研究数据:在既往至少一线系统治疗失败的携带KRAS G12C突变的晚期NSCLC受试者中开展的单臂II期注册临床研究,共有116例受试者纳入分析。独立影像学评审委员会评估的ORR达46.6%,疾病控制率达90.5%,中位缓解持续时间为8.3个月,中位PFS 为8.3个月(95%CI: 5.6-10.4),中位OS尚未达到。IBI351总体耐受性良好,最常见的治疗相关AE为贫血、谷丙转氨酶升高、谷草转氨酶升高、乏力和蛋白尿。3级及以上AE发生率为40.5%。
既然有临床试验新药治疗的机会,那么如何鉴定KRAS突变状态,评估患者是否存在KRAS G12C这一重要靶点呢?
基因检测已经成为NSCLC精准诊治的重要环节。NGS、荧光定量PCR和Sanger测序是检查KRAS突变状态最常用的方法,首选利用肿瘤组织进行基因检测。当组织样本不可获得的情况下,也可以利用外周血进行NGS检测评估是否存在KRAS G12C突变。笔者前期接诊过几例晚期肺癌患者,既往虽然进行了肺癌基因检测,但利用一代测序或ARMS法,并未找到潜在获益的基因突变。和患者沟通后利用气管镜检再次活检以及NGS分析,帮助患者明确携带KRAS G12C突变,最终参加KRAS G12C新药临床试验获得病情缓解。

图例为1例肺腺癌组织样本NGS检测方法提示KRAS G12C突变
另一例晚期NSCLC(腺癌)患者,既往采用荧光定量PCR方法(ADX-ARMS法)仅发现存在KRAS突变,无法进一步区分突变位点,我们用Q-PCR方法帮助患者用远低于NGS的费用明确了KRAS G12C突变。
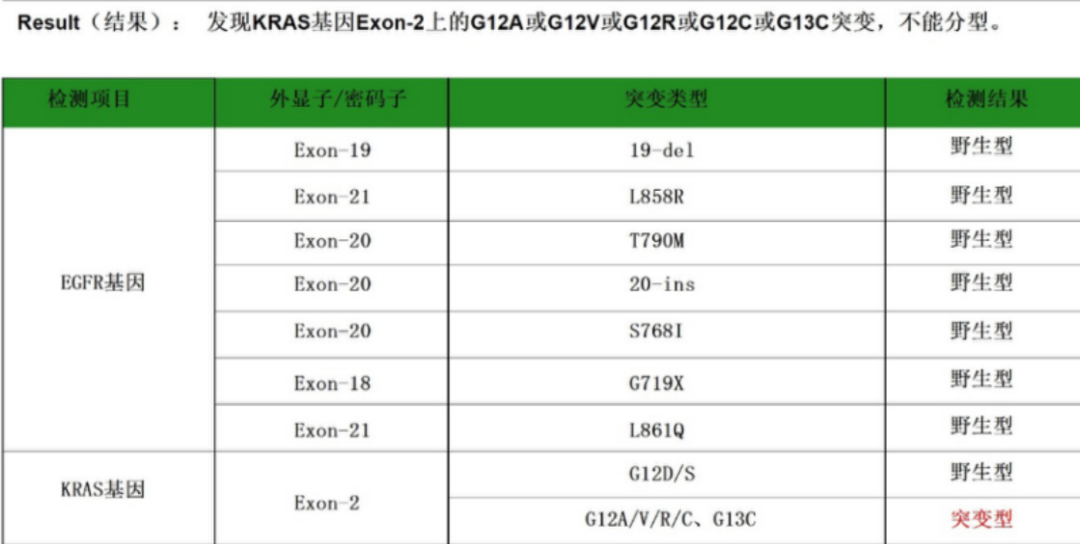
A 荧光定量PCR方法(ADX-ARMS法)报告
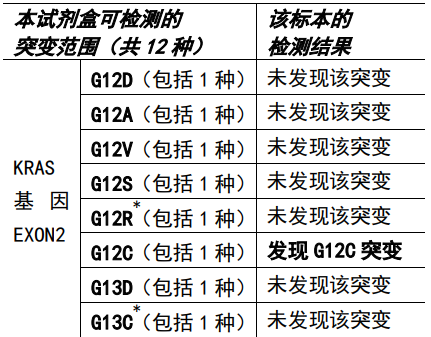
B Q-PCR方法进一步确定突变类型为KRAS G12C突变
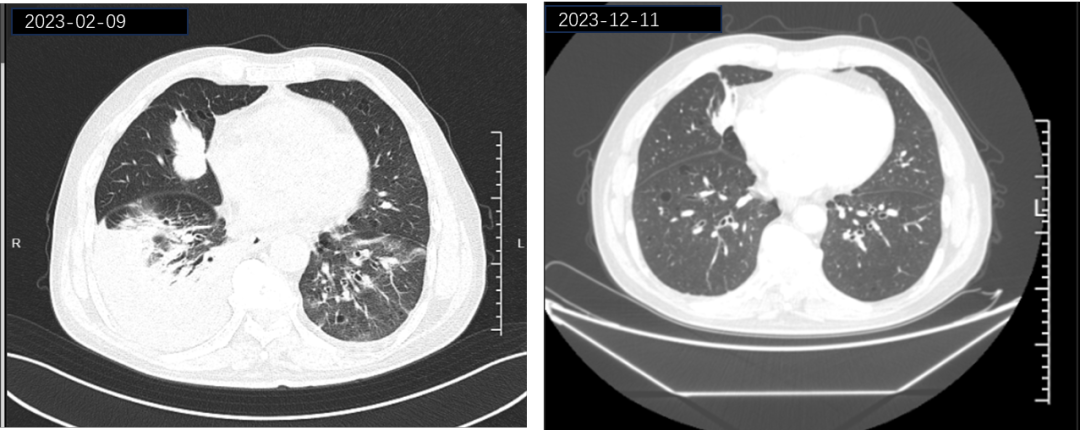
该患者经过含铂化疗联合免疫治疗以及放疗后疾病进展,合并多发骨转移、中度贫血及癌痛。当确诊KRAS G12C突变之后,患者又面临药物不可及的困难。我们一方面鼓励患者筛选参加KRAS G12C抑制剂临床试验,一方面给予支持治疗控制癌痛、处理前期治疗造成的贫血等不良反应。最终顺利地帮助患者筛选入组临床新药治疗,取得显著的肿瘤缓解。如下图所示,患者服药10月后的复查提示胸腔积液较用药前明显吸收,肿瘤退缩后患者咳嗽及疼痛等症状明显改善,目前仍在定期接受免费的KRAS G12C抑制剂靶向治疗。
综上,KRAS突变是晚期肺癌中的常见驱动因子,目前治疗面临较大挑战,传统化疗效果有限。针对KRAS突变的靶向药物开辟了新的治疗前景,尤其是特定亚型如KRAS G12C抑制剂的问世,预示着难治性肺癌精准治疗的新时代。“精准治疗,诊断先行”,基因分析对鉴定患者的KRAS突变状态、预后评估、指导治疗方案具有重要影响。在科学进步的助力下,我们有理由保持乐观,伴随这一新兴治疗的力量,一起努力赢得健康的未来,期待更多顽强的生命奇迹绽放!
本文作者:

生金 教授
肿瘤学博士、临床医学博士后
浙江大学医学院附属邵逸夫医院肿瘤内科 副主任医师
中国医药教育协会腹部肿瘤医学综合康复分会委员
中国抗癌协会多原发和不明原发肿瘤专业委员会专业会员
浙江省抗癌协会肿瘤内科青年委员会委员
浙江省健康科普专家库肿瘤防治科普分库成员
浙江省数理医学学会抗肿瘤药物临床研究专委会委员
发表SCI论文10余篇,参与国际/国内多中心实体瘤药物临床研究50余项,主持国家自然科学基金青年项目1项、参加国自然面上项目1项,主持浙江省博士后择优资助项目1项
版权声明
以上内容来自良医汇-肿瘤医生APP,如有建议或疑问,欢迎致电021-64360386。
 长按二维码
长按二维码关注精彩内容






