诺华12月9日宣布VAYHIT2三期临床试验取得积极结果,该试验评估了ianalumab联合艾曲泊帕在既往接受糖皮质激素治疗的原发性免疫性血小板减少症(ITP)患者中的疗效和安全性。Ianalumab(9 mg/kg)联合艾曲泊帕将ITP疾病控制延长了45%,该结果基于主要研究终点“至治疗失败时间(TTF, Time To Treatment Failure)”,即评估患者在治疗期间及治疗后维持安全血小板水平的时间。接受ianalumab联合艾曲泊帕治疗的患者,其至治疗失败的中位时间是安慰剂联合艾曲泊帕组的2.8倍(13.0个月 vs 4.7个月)。
详细数据于第67届美国血液学会年会(ASH)的最新突破摘要(Late-Breaking Abstracts) 专场公布,并同步发表于《新英格兰医学杂志》。
“ITP的治疗一直以来侧重于提升血小板计数,通常需要长期治疗以控制疾病。这意味着许多患者需要长期用药,持续承受疾病负担和如疲劳等的症状。”麻总百瀚医院(Mass General Brigham)血液学/肿瘤学Peggy S. Blitz讲席教授、哈佛医学院医学副教授Hanny Al-Samkari博士表示,“VAYHIT2试验结果令人鼓舞,显示即使在患者停药期间也能实现更好的疾病控制,为ITP患者带来新的希望。”
接受ianalumab(9 mg/kg)联合艾曲泊帕治疗的患者,在第6个月时持续血小板计数改善的比例也显著高于安慰剂联合艾曲泊帕治疗组(62% vs 39%),达到了关键次要终点。疲劳改善方面,PROMIS疲劳评分显示,ianalumab联合艾曲泊帕组平均下降7.7分,安慰剂联合艾曲泊帕治疗组下降3.6分。
“B细胞驱动的自身免疫反应导致ITP患者血小板破坏和出血风险增加。Ianalumab的创新双重作用机制旨在清除B细胞并阻断其存活信号。”诺华全球肿瘤开发负责人Mark Rutstein博士表示,“凭借我们在ITP领域多年的经验,VAYHIT2结果进一步证明ianalumab有望通过每月一次、共四次的静脉输注方案,实现持久疾病控制,让患者无需长期持续治疗。”
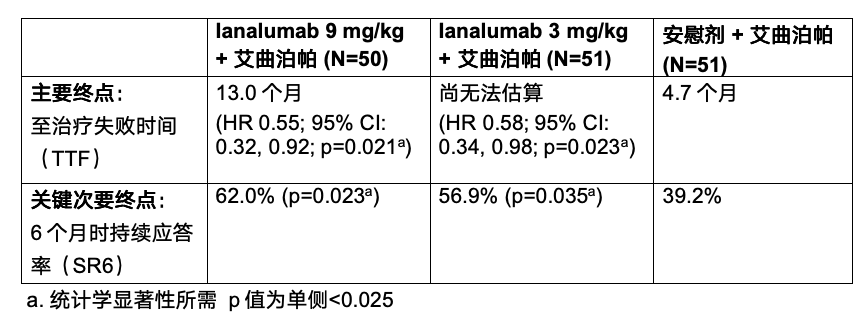
VAYHIT2评估了两种剂量的ianalumab,其中9 mg/kg剂量在主要和关键次要终点均显示出统计学显著改善,3 mg/kg剂量在主要终点达到统计学显著,关键次要终点有数值改善。
Ianalumab耐受性良好,未发现新的安全信号,安全性与既往研究一致。Ianalumab组与安慰剂组的不良事件发生率相当,最常见的不良事件为头痛(9 mg/kg组14%,3 mg/kg组10%,安慰剂组8%)和输注相关反应(9 mg/kg组14%,3 mg/kg组8%,安慰剂组8%)。中性粒细胞减少症在ianalumab组更常见(9 mg/kg组16%,3 mg/kg组12%,安慰剂组2%),大多数病例无需治疗或剂量调整即可恢复。未有因治疗期间不良事件导致永久停药的情况。
VAYHIT2是ianalumab的第三项获得阳性结果的III期临床试验,此前在活动性干燥综合征成人患者中已有两项阳性结果。诺华计划于2027年将VAYHIT2数据与正在进行的一线ITP试验结果(VAYHIT1)一同提交。Ianalumab已获得美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)的孤儿药资格认定。(来源:诺华中国)
(注: 此文属于央广网登载的商业信息,文章内容不代表本网观点,仅供参考。)
 长按二维码
长按二维码关注精彩内容






